Регуляция активности ферментов может осуществляться путём взаимодействия ферментов с различными биологическими компонентами или чужеродными соединениями, которые называются регуляторами ферментов. Они могут либо ускорять, либо замедлять ферментативную реакцию.
Активаторы ферментов
– это вещества, увеличивающие скорость ферментативной реакции.
Виды активаторов:
1. Вещества, влияющие на область активного центра. К ним относятся ионы металлов (Na+, K+, Fe2+, Co2+, Cu2+, Ca2+, Zn2+, Mg2+, Mn2+ и др.). В ряде случаев ионы металлов выполняют функцию кофактора фермента. В других случаях они способствуют присоединению субстрата к активному центру фермента. Ионы металлов оказываются активаторами только в условиях дефицита их в организме.
2. Аллостерические эффекторы, которые связываются с аллостерическим (регуляторным) участком апофермента. Это связывание вызывает конформационные изменения в молекуле белка, приводящие к изменению структуры активного центра, что сказывается на связывании и превращении субстрата в активном центре. При этом активность фермента либо увеличивается (это аллостерические активаторы), либо уменьшается (это аллостерические ингибиторы). Аллостерическими эффекторами ферментов наиболее часто выступают различные метаболиты, а также гормоны, ионы металлов, нуклеозиды - АТФ, АДФ, АМФ.
3. Вещества, вызывающие модификации, не затрагивающие активный центр фермента. Возможно несколько вариантов таких модификаций:
- активация путём присоединения специфической модифицирующей группы к молекуле фермента.
Отрицательно заряженные фосфатные группы могут разрывать слабые водородные и ионные связи в третичной структуре белка-фермента и влиять на конформационное состояние его активного центра. В зависимости от природы фермента фосфорилирование может его активировать или, наоборот, инактивировать. Реакции присоединения фосфатной группы катализируют ферменты протеинкиназы, а отщепления – фосфатазы. Активность этих ферментов в свою очередь находится под контролем гормональной системы.
- активация путём перехода неактивного предшественника - профермента в активный фермент за счёт частичного протеолиза.
Некоторые ферменты синтезируются в клетке первоначально неактивными и после секреции из клетки переходят в активную форму. Неактивные предшественники называются проферменты (зимогены). Под действием активатора происходит частичный гидролиз профермента с отщеплением от него неактивного пептида, в результате чего открывается активный центр. Так происходит активация ферментов желудочно-кишечного тракта, переваривающих белки пищи. Например, фермент пепсиноген, синтезированный в клетках желудка, затем в просвете желудка под действием соляной кислоты превращается в активный пепсин путём удаления неактивного участка полипептидной цепи:
- активатор вызывает диссоциацию субъединиц фермента, имеющего четвертичную структуру (отщепление одной из субъединиц фермента).
Ингибиторы ферментов
Ингибиторами называют вещества, вызывающие снижение активности фермента. Следует различать инактивацию и ингибирование фермента. Сам по себе факт торможения ферментативной реакции в присутствии какого-либо вещества ещё не говорит о том, что это вещество – ингибитор. Любые денатурирующие агенты вызывают инактивацию фермента и торможение ферментативной реакции. Ингибиторы, в отличие от денатурирующих агентов, действуют в малых концентрациях и вызывают специфическое снижение ферментативной активности.
По прочности связывания с ферментом ингибиторы делятся на обратимые и необратимые. Необратимые ингибиторы прочно связываются с ферментом, тогда как комплекс фермент – обратимый ингибитор непрочен. Если сильно разбавить раствор фермента с обратимым ингибитором, то их комплекс распадается и активность фермента восстанавливается.
Механизмы действия ингибиторов ферментов
По механизму действия ингибиторы делятся на конкурентные и неконкурентные.
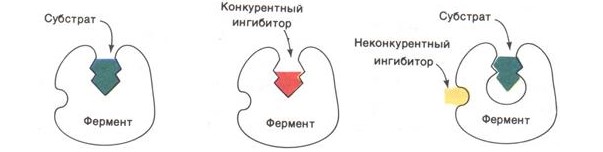
Конкурентные ингибиторы имеют структурное сходство с молекулой субстрата, что позволяет им занять место субстрата в активном центре фермента:
E + S + I → EI + S
Встраиваясь вместо субстрата в активный центр, такой ингибитор не даёт ферментативной реакции осуществиться. То есть, субстрат конкурирует с ингибитором за активный центр. С активным центром связывается то соединение, молекул которого больше. Снять конкурентное ингибирование можно, увеличив концентрацию субстрата.
На принципе конкурентного ингибирования основано действие многих фармакологических препаратов (например, сульфаниламидных), инсектицидов, фосфорорганических боевых отравляющих веществ (зарин, зоман).
Неконкурентные ингибиторы не имеют структурного сходства с субстратами. Они или связываются с каталитическими группами активного центра фермента, или, связываясь с ферментом вне активного центра, изменяют конформацию активного центра таким образом, что это препятствует превращению субстрата. Поскольку неконкурентный ингибитор не влияет на связывание субстрата, то в отличие от конкурентного ингибирования наблюдается образование тройного комплекса:
E + S + I → ESI
К неконкурентным ингибиторам относятся ионы тяжёлых металлов: ртути, свинца, кадмия, мышьяка. Они блокируют SH-группы, входящие в каталитический участок фермента. Снять действие неконкурентного ингибитора избытком субстрата, как при конкурентном ингибировании, нельзя, а можно лишь веществами, связывающими ингибитор (реактиваторами). Тяжелые металлы лишь в небольших концентрациях играют роль ингибиторов, в больших концентрациях они действуют как денатурирующие агенты.
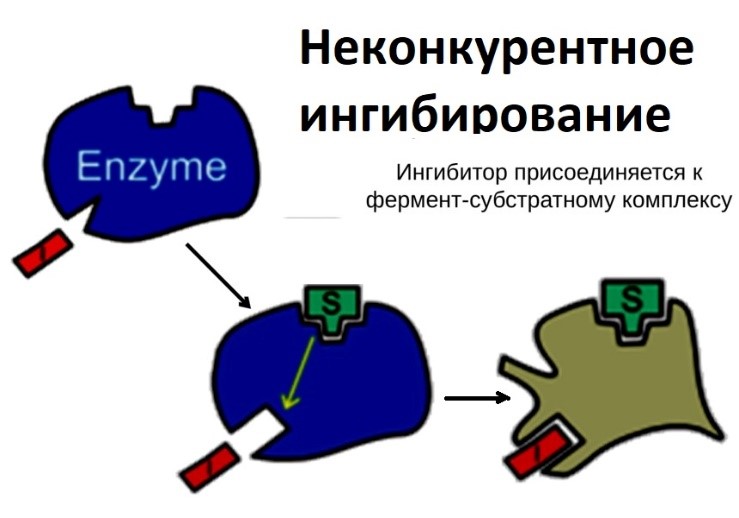 Наиболее важными неконкурентными ингибиторами являются образующиеся в живой клетке промежуточные продукты метаболизма, способные обратимо связываться с аллостерическими участками фермента – аллостерические ингибиторы.
Наиболее важными неконкурентными ингибиторами являются образующиеся в живой клетке промежуточные продукты метаболизма, способные обратимо связываться с аллостерическими участками фермента – аллостерические ингибиторы.
Они занимают ключевое положение в метаболизме, поскольку тонко реагируют на изменения в обмене веществ и регулируют прохождение веществ по целой системе ферментов.
Например, аллостерическая регуляция проявляется в виде ингибирования конечным продуктом первого фермента цепи. Эта регуляция сходна с регуляцией по механизму обратной связи и позволяет контролировать выход конечного продукта, в случае накопления которого прекращается работа первого фермента цепи